240510投稿
ストレスによって誘導されるheterochromatin構造の変化が後代に伝わる
次に、前に紹介した、親への糖負荷が子孫にepigeneticallyに伝わるという研究論文に関連して、マウスを使った石井俊輔のグループの研究(文献10)を取り上げるつもりだった。しかし、その前に、石井グループ(理研つくば)の関連分野を代表する先駆的研究(文献11)解説することにした。
転写調節因子Drosophila ATF-2はheterochromatin構築を支配し、ストレスによってATF-2がリン酸化されるとheterochromatin構造が壊れ、隠されていた遺伝子の発現が起こる。このheterochromatinによって隠される部位にw遺伝子(発現すると眼の色が赤になる)をはめこんで、ストレスによって眼が赤くなる系wm4は、前回紹介したÖstの研究(文献8)でも利用していた。
ハエの培養細胞株S2をheat shockあるいはosmotic shockにさらすと、p38が活性化され、dATF-2のリン酸化さ起こる。Wm4ハエの産卵後0-3hrのembryoを高温処理し、羽化してからw遺伝子のsilencingを調べたところ、弱まっていた。産卵後3hrを過ぎるとheat shockの効果が見られなかった。Embryoをheat shockすると、抽出液の核分画に含まれるdATF-2が減った。HS後すみやかに核から遊離したP-dATF-2の量が増えるが、その後急速に減じた(分解された)。TOPRO-3染色で見ると、HS後、heterochromatinシグナルのサイズが減少した。同じようなHSによる変化はprimordial germ cellsにも認められた。
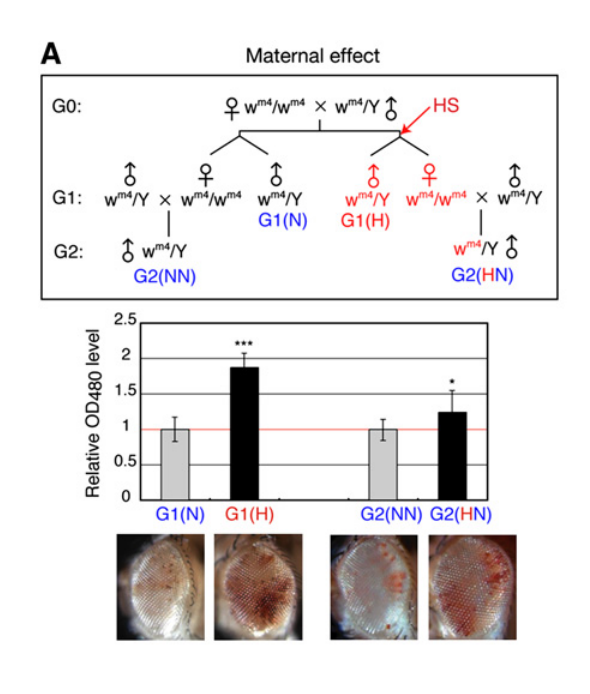
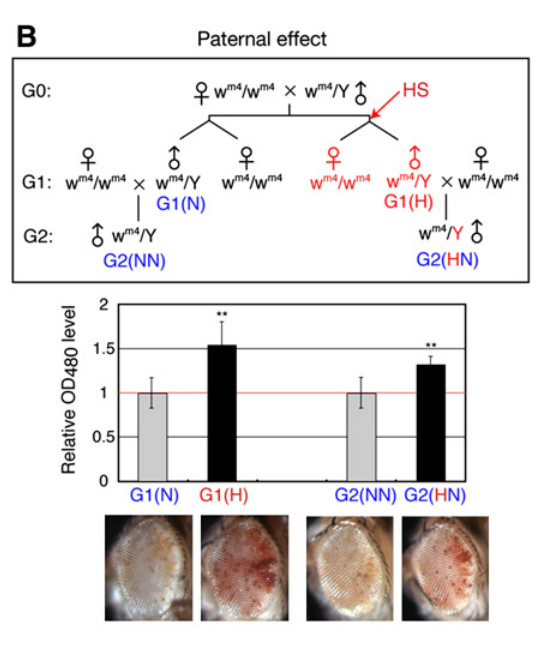
HSによって生殖細胞でheterochromatin構築が壊れるとすると、その変化が子孫に伝わる可能性があるので、調べてみた。wm4 embryosをHS処理し、生まれてきた♀ハエを普通の♂ハエと交配した。生じた(Fig.1の右下w4m/Y)♂ハエの眼の色は赤色化、つまりheterochromatinによるw遺伝子の発現抑制が解除されていた(Fig.1)。親(G1)が受けたHSの効果がw4mを通じて仔(G2)に伝達されたと考えられる。ところが、不思議なことに、w4m embryoをHS処理して生まれた♂ハエを普通の♀ハエと交配して作ったG2♂ハエでもw遺伝子の抑制が弱くなっていた(赤眼になった)。G2♂の性染色体はw4m/Yであるから、w遺伝子の発現を抑制していたheterochromatin構造はHSにさらされていない。石井らは、この結果を非メンデル様式と称し、染色体間で影響しあうparamutationの類と指摘した。HSの代わりにosmotic stressを使っても、同様にstressによるheterochromatinの弱体化は次世代に伝達された。
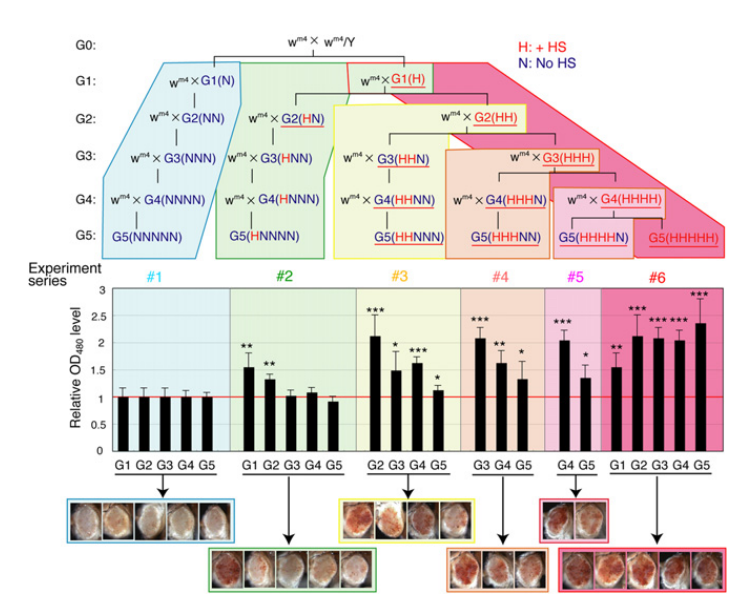
HS処理の効果が次世代以降の子孫に伝わるかどうかを調べた。Fig.3を見てみる。まず、HS処理したembryoから生じたG1♀をHS処理してない♂と交配して生まれたG2のw遺伝子が少し発現したことは、上に述べた。HS処理G1♀とN(normal) ♂を交配して作ったG2 embryoをそのまま発生羽化させたG2ハエでも弱いながらもw遺伝子の発現が認められた。同じembryoをHS処理し、G2ハエを作ったところ、w遺伝子の発現抑制がさらに強く解除された(Fig.3の左から3番目のグラフ)。同様に、HS処理G2♀とN♂を交配し、G3 embryoを作った。そのまま羽化成体化させ、G3♀とN♂を交配させた。以下同様にG5までの結果を得た(Fig.3)。結果は、世代を続けてHS処理すると、w遺伝子の発現はますます強くなる(heterochromatinによる抑制が解除される)ことが明らかとなった。壊れたheterochromatinの状態はHS処理しなくても、程度に応じて次世代、次々世代まで伝達された。
dATF-2がheterochromatin形成を通じて、実際にどのような遺伝子(w遺伝子はモデル)の発現を抑制しているかを調べた。HS処理したG1♂とN♀を交配して作ったG2ハエと無処理のハエの遺伝子発現をmicroarray解析で比較した。HS処理で97 genesが発現増加した。この97 genesのうち88 genesのupregulationはdATF-2欠損株では認められなかった。さらに、88 genes中20 genesはHSと関係なく、dATF-2変異株でupregulatedされていた。すなわち、これらのgenesの発現がdATFによって直接抑制されていることを示唆している。
このブログの観点からみて、本論文には面白い点が2つある。第一に、HS処理の効果が多世代にわたって子孫に影響をおよぼすが、その効果は世代を重ねるとなくなることである。第二は、HSを受けた♂ハエとN♀と交配してできた♂とN♀を交配してできた♂ハエ(HSを受けたX染色体をもたない)に、w遺伝子の抑制解除が認められてことである。著者たちが論じているように、HSの効果がtransに作用したことになる。Transに作用するparamutationの場合、低分子RNAの関与が示唆されている研究もあり、石井らの文献10の研究は、この点にも踏み込んであり、重要な知見となっている。次回に、紹介する。
- Yoshida, K., et al. Mol Cell 78: 445 (2020)
- Seong, K-H. et al. Cell 145: 1049 (2011)